| Feladat: | 2550. fizika feladat | Korcsoport: 18- | Nehézségi fok: átlagos |
| Füzet: | 1991/november, 421. oldal |  PDF | PDF |  MathML MathML |
|
| Témakör(ök): | Kristályos anyagok, Feladat | ||
| Hivatkozás(ok): | Feladatok: 1991/február: 2550. fizika feladat | ||
|
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. A tércentrált köbös szerkezetű kristályok elemi cellája kocka alakú, és az atomok a kocka középpontjában és csúcsaiban helyezkednek el. Minthogy a csúcsokban nyolc szomszédos cella találkozik, az itt elhelyezkedő atomoknak csak -ad része esik egy cellába. Így egy cellához atom tartozik. 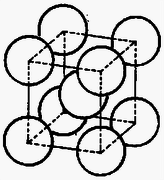 1. ábra 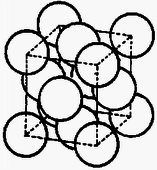 2. ábra A felületen centrált köbös szerkezetben a legközelebbi atomok az elemi cella lapátlója mentén találhatók (2. ábra). Így az elemi cella élhossza , térfogata pedig . A felületen centrált köbös szerkezetű vas ,,atomsűrűsége'': . Mivel az atomsűrűségek arányosak a sűrűségekkel, a relatív sűrűségváltozás A sűrűség tehát mintegy -kal csökkent. |