|
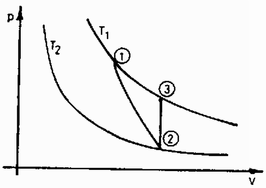
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. A két folyamatot diagrammon ábrázolva láthatjuk, hogy a kezdeti és a végállapotban a gáz ugyanazon az izotermán helyezkedik el.
A gáz belső energiája tehát azonos az 1. és a 3. állapotban: Ebből következik, hogy az 1‐2 átmenet során a belső energia változása megegyezik a 2‐3 átmenethez tartozó belső energia változással, de azzal ellentétes előjelű: | | (2) |
A második átmenet során a gáz térfogata nem változik, így . Az adatok alapján , . Ezeket az értékeket (2)-be helyettesítve adódik, hogy:
Ezt az eredményt felhasználva már könnyű meghatározni a mólhőt. Ha egy folyamatban egy mólnyi gáz hőmérséklete -ről -re változik, akkor A két hőmérséklet különbsége a második folyamatból meghatározható: Mivel ismert , ezért (4) és (5) felhasználásával a keresett mólhő: | |
Az az érdekes eset állt elő, hogy a gázzal hőt közlünk (+40 J), de a hőmérséklete mégis csökken (hiszen sok munkát is végez). Ezért a folyamathoz tartozó mólhő negatív.
Vass Gergely (Sopron, Széchenyi I. Gimn., I. o. t.)
|
|
 PDF |
PDF |  MathML
MathML