| Feladat: | 2123. fizika feladat | Korcsoport: 16-17 | Nehézségi fok: átlagos |
| Megoldó(k): | Csordás Zoltán Mihály | ||
| Füzet: | 1987/március, 136 - 137. oldal |  PDF | PDF |  MathML MathML |
|
| Témakör(ök): | Fázisdiagram, Kémiával kapcsolatos feladatok, Feladat | ||
| Hivatkozás(ok): | Feladatok: 1986/április: 2123. fizika feladat | ||
|
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. A kétkomponensű rendszerek legegyszerűbb példái a sóoldatok. Ezek jellemző fázisdiagramja az ábrán látható. A függőleges tengelyre a hőmérsékletet, a vízszintesre az összetételt mértük fel. 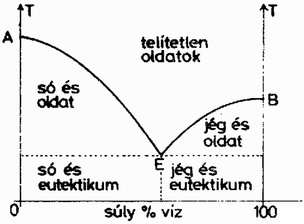 Az görbe a fagyáspont változását mutatja az összetétel függvényében. (Fagyáspont az a hőmérséklet, amelyen az első kristályok megjelennek.) a tiszta só, a tiszta víz fagyáspontja. Pl.: Az görbe mentén két fázis, a telített sóoldat és a szilárd só van egyensúlyban. Ahogyan növeljük az oldat víztartalmát, a fagyáspont csökken, mígnem az eutektikus ponthoz érünk. E folyamat során az oldat a sóra nézve hígul, a vízre nézve töményedik, és az pontban lesz telített a vízre is. Az ponthoz tartozó összetételű oldatot eutektikus összetételűnek nevezzük. Az -hez tartozó hőmérséklet (eutektikus hőmérséklet) alatti só és jégkristály keveréket nevezzük eutektikumnak. A keverék teljes megszilárdulása után az eutektikum finom kristályaiba beépülve a fölöslegben levő komponens nagy kristályai válnak ki. Az eutektikumok igen alkalmasak alacsony hőmérsékletek előállítására. Ha szilárd sót és jeget az eutektikumnak megfelelő arányban keverünk, akkor a hőmérsékletük leszáll az eutektikus hőmérsékletre. A só ugyanis a jég felületén megolvadt vízrétegben feloldódik. E tömény sóoldattal az eredetileg C-os jég nincs egyensúlyban, ezért olvadásnak indul. (Mivel a só oldódása, illetve az olvadás csak a jég felületén történik, előnyös az utóbbit nagy felületű alakban alkalmazni (hó, darált jég).) Olvadás közben a jég az olvadáshőt elvonva a rendszertől azt addig hűti, míg elő nem áll az eutektikus hőmérséklet. Ily módon tehát a jég egyszerű sózásával alacsony hőmérséklet állítható elő, természetesen megfelelő mennyiségű jég megolvadása árán. Csordás Mihály Zoltán (Esztergom, Dobó K. Gimn., I. o. t.) |