|
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. A gáz hőmérsékletének emeléséhez a termodinamika I. főtétele értelmében hőre van szükség, ahol a gáz belső energiájának megváltozása, pedig a gázon végzett munka a két állapot közötti átmenet során.
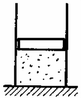 a)
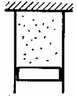 b)
Ismeretes, hogy az termodinamikai szabadságfokkal bíró, részecskéből álló ideális gáz belső energiáját valamely hőmérsékleten az kifejezés adja meg ( a Boltzmann-állandó). Állandó nyomáson végbemenő (izobár) folyamatoknál a gázon végzett munka ha a gáz térfogatváltozása . A (2) és (3) kifejezést az (1) összefüggésbe helyettesítve a következő összefüggést kapjuk:
Ez az egyenlőség adja meg az ideális gáz izobár állapotváltozása során a rendszer által felvett (leadott) hőt.
Az ábra szerinti a) és b) esetben a gáz nyomása különböző. (, illetve , ahol a külső levegő nyomása, a dugattyú súlyából adódó nyomás.) Állandó belső nyomás esetén azonban a végzett tágulási munka nagysága független a nyomás értékétől. Az ideális gáz állapotegyenlete, alapján állandó nyomás esetén ugyanis Ezt a (4) egyenletbe írva: | | (6) |
Látható, hogy a kívánt hőmérséklet-növekedéshez a gázzal közlendő hő csak a hőmérséklet-növekedéstől függ, így mindkét esetben ugyanakkora hő szükséges.
A (6) összefüggésből leolvasható az állandó térfogathoz, ill. nyomáshoz tartozó , ill. hőkapacitás definíciója is.
|
|
 PDF |
PDF |  MathML
MathML 
