| Feladat: | 1454. fizika feladat | Korcsoport: 16-17 | Nehézségi fok: nehéz |
| Megoldó(k): | Bene Gyula , Benkő Zsigmond , Kaufmann Zoltán , Tél Tamás | ||
| Füzet: | 1978/március, 133 - 137. oldal |  PDF | PDF |  MathML MathML |
|
| Témakör(ök): | Adiabatikus állapotváltozás, Gázok egyéb állapotváltozása, Egyéb (gázok fajhőjével kapcsolatos), I. főtétel, Ideális gáz állapotegyenlete, Ideális gáz belső energiája (Állapotegyenletek), Függvényvizsgálat differenciálszámítással, Feladat | ||
| Hivatkozás(ok): | Feladatok: 1977/október: 1454. fizika feladat | ||
|
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. I. megoldás. Az egyszerűség kedvéért tegyük föl, hogy egy mólnyi ideális gázt vizsgálunk, s legyen az állandó térfogat mellett mért mólhő . 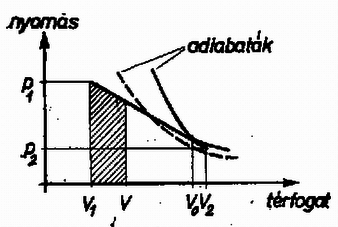 A folyamatot a síkon az 1. ábrán látható grafikon szemlélteti. Ennek megfelelően az állapotváltozás egyenlete
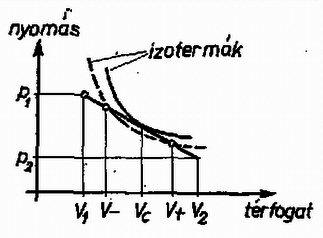 E két tartományt olyan pont választja el, ahol a két meredekség egyenlő. Határozzuk meg most ezen pont koordinátáját! Ideális gáz adiabatájának egyenlete (l. Budó: Kísérleti fizika I.):
Ezek után már választ tudunk adni a feladat első kérdésére. Amennyiben az adatok olyanok, hogy
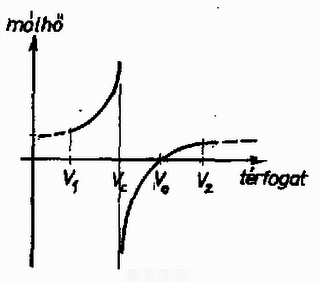 A következő lépés a fajhő meghatározása. Az 1329. feladatban [KML 52 (1976) 230. old.] ugyanezen folyamat fajhőjét kiszámoltuk (csak ott pozitív volt), ezért itt most egyszerűen idézzük az ottani eredményt (javasoljuk az olvasóknak, hogy tanulmányozzák át a részletes levezetést). A mólhő a folyamat során pontról pontra változik; s amikor a rendszer térfogata , akkor
II. megoldás. Azt, hogy a folyamat melyik részén történik hőfelvétel, úgy is meghatározhatjuk, hogy megvizsgáljuk, mennyi hőt vesz fel a rendszer a térfogat eléréséig. Ha ismerjük az ezt leíró függvényt, akkor már meg tudjuk adni a kívánt választ. Tekintsünk ugyanis egy értéket! Ha ennél -vel nagyobb térfogathoz nagyobb hő tartozik, mint a kiindulási, vagyis ha Ennek deriváltja:
Bene Gyula (Miskolc, Földes F. Gimn., III. o. t.) dolgozata alapján III. megoldás. A hőfelvételi és hőleadási tartományokat elválasztó pont az alapján is meghatározható, hogy ott a mólhő előjelet vált úgy, hogy folytonosan megy át pozitívból negatív értékbe, vagy fordítva. (Az 1. megjegyzésben látni fogjuk, hogy előfordulhat nem folytonos előjelváltozás is.) A (8)-ban felírt függvény zérushelyére a következő feltételt kapjuk: Megjegyzések. 1. Bene Gyula észrevette, hogy a mólhő (8) kifejezése a A pont közvetlen környezetében a rendszer hőmérséklete nem változik, hőközlés azonban történik, hiszen munkavégzés van, s ez mind hővé alakul, így érthető, hogy ez formálisan végtelen nagy fajhő megjelenésében mutatkozik meg. Az is világos, hogy a fajhő előjele itt megváltozik: , és összehasonlításából közvetlenül látszik, hogy mindig kisebb, mint . Az előzőekben megmutattuk, hogy -ig hőfelvétel történik. A térfogatot növelve először a hőmérséklet is nő, így a fajhő pozitív lesz. értékét átlépve azonban a hő továbbra is pozitív, de a hőmérséklet-különbség negatívvá válik, így a fajhő is negatív lesz. Először nagyon nagy érték, s fokozatosan csökken. után már a felvett hő is előjelet vált, így ismét pozitív fajhőt kapunk. Arra az esetre, amikor a és értékek a intervallumba esnek, a 3. ábra mutatja a mólhő függését a állapotjelzőtől. A mólhő tehát előjelet vált a pontban is, de itt végtelen nagy ugrása is van, hiszen a hőmérséklet-változás körül nulla. Az ilyen típusú előjelváltás azonban nem jelenti azt, hogy a hőfelvétel is előjelet vált, ellenkezőleg, amiatt lép föl, hogy a hőfelvétel előjele változatlan, de a hőmérséklet-különbség előjele megcserélődik. Annak ellenére, hogy a mólhő -ben végtelen, a hőfelvétel mégis véges, amit jól mutat az, hogy a függvény nem válik végtelenné ezen a helyen. 2. Sok megoldó a pontot tekintette a hőfelvétel előjelváltását leíró adatnak. Ez valószínűleg abból adódik, hogy nem különböztetik meg élesen a hő és hőmérséklet fogalmát. A pont körül ‐ mint láttuk ‐ hőmérséklet-különbség nem lép fel, de hőátadás igenis van. E két mennyiség tehát csak speciális esetekben arányos egymással, pl. folyadék melegítésekor, de sok más esetben függetlenek. (A magyar nyelvben egyébként az ilyen típusú szópárok két tagjának eltérő értelme van. A hő és hőmérséklet között legalább akkora a különbség, mint a vér és vérmérséklet szavak jelentése között.) 3. A megoldók nagy része úgy akarta kiszámolni a folyamat során közölt hőt, hogy egy izochor és egy izobár folyamat összegét vizsgálta. Sokszor leírtuk már, de álljon itt még egyszer: a hő és a munkavégzés nem állapotjelzők (ismét egy különbség a hő és hőmérséklet között!), ezért nem csak a kezdő és végállapottól függnek. |