| Feladat: | 421. fizika feladat | Korcsoport: 16-17 | Nehézségi fok: nehéz |
| Megoldó(k): | Babai László | ||
| Füzet: | 1964/szeptember, 44 - 45. oldal |  PDF | PDF |  MathML MathML |
|
| Témakör(ök): | Ideális gáz állapotegyenlete, Kémiával kapcsolatos feladatok, Feladat | ||
| Hivatkozás(ok): | Feladatok: 1964/január: 421. fizika feladat | ||
|
A szöveg csak Firefox böngészőben jelenik meg helyesen. Használja a fenti PDF file-ra mutató link-et a letöltésre. Számítsuk ki, hány liter maradt az üvegben, miután liter szódavizet kiengedtünk. A térfogatot 1 atm nyomásra és szobahőmérsékletre adjuk meg. Henry törvénye szerint az oldott gáztérfogat: Ha liter szódavizet kiengedünk, a maradékban ( liter 1 atm nyomású gáznak megfelelő mennyiség lesz. Feltételezzük, hogy a gyors kieresztés következtében a gáztérből nem távozott el semmi, és a kiengedett szódavíz a atm nyomásnak megfelelő oldott mennyiséget tartalmazza. A maradék gáz térfogata tehát:
dolgozata alapján. 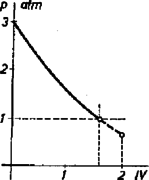 Megjegyzés. Ha a nyomás az üvegben egyenlő lesz a külső nyomással, több vizet már nem engedhetünk ki belőle. A fenti végképletben atm-t helyettesítve, megkaphatjuk az üvegből maximálisan kiengedhető szódavíz térfogatát: Vermes Miklós |